Респираторный дистресс-синдром
 Синдром острых дыхательных расстройств или респираторный дистресс-синдром (РДС, Acute respiratory distress syndrome ARDS –англ.) у взрослых в настоящее время заменил собой термин «шоковое легкое» — специфическую форму острых дыхательных нарушений, сопутствующих многим формам критических состояний (шок, ингаляция раздражающих газов, аспирационные и вирусные пневмонии, острый панкреатит, язвенный колит). Своеобразие термина определяет сходство синдрома по основным клинико-морфологическим данным с паренхиматозной дыхательной недостаточностью у детей, рожденных в состоянии асфиксии. В обоих вариантах нарушается полноценность сурфактанта — поверхностно-активного вещества, поддерживающего альвеолы в расправленном состоянии. После тяжелых ранений и травм респираторный дистресс-синдром (РДС) наблюдается в среднем в 6% всех случаев. Относительно чаще респираторный дистресс-синдром осложняет тяжелые повреждения груди (закрытые травмы, проникающие ранения), а также ЧМТ тяжелой степени. РДС может развиться и при ранениях шеи, живота, конечностей, когда они сопровождаются шоком и требуют переливания больших объемов жидкости, крови. Летальность при РДС достигает 75%. В поздние сроки респираторный дистресс-синдром чаще развивается в связи с возникновением сепсиса, первичным очагом для которого обычно является гнойно-инфекционный процесс в легких, брюшной полости.
Синдром острых дыхательных расстройств или респираторный дистресс-синдром (РДС, Acute respiratory distress syndrome ARDS –англ.) у взрослых в настоящее время заменил собой термин «шоковое легкое» — специфическую форму острых дыхательных нарушений, сопутствующих многим формам критических состояний (шок, ингаляция раздражающих газов, аспирационные и вирусные пневмонии, острый панкреатит, язвенный колит). Своеобразие термина определяет сходство синдрома по основным клинико-морфологическим данным с паренхиматозной дыхательной недостаточностью у детей, рожденных в состоянии асфиксии. В обоих вариантах нарушается полноценность сурфактанта — поверхностно-активного вещества, поддерживающего альвеолы в расправленном состоянии. После тяжелых ранений и травм респираторный дистресс-синдром (РДС) наблюдается в среднем в 6% всех случаев. Относительно чаще респираторный дистресс-синдром осложняет тяжелые повреждения груди (закрытые травмы, проникающие ранения), а также ЧМТ тяжелой степени. РДС может развиться и при ранениях шеи, живота, конечностей, когда они сопровождаются шоком и требуют переливания больших объемов жидкости, крови. Летальность при РДС достигает 75%. В поздние сроки респираторный дистресс-синдром чаще развивается в связи с возникновением сепсиса, первичным очагом для которого обычно является гнойно-инфекционный процесс в легких, брюшной полости.
Главным звеном в патогенезе РДС служат возрастающая проницаемость легочных капилляров и накопление жидкости в просвете альвеол, воздухоносных путях, что сопровождается бронхоспазмом. Отправной точкой для развития патологических расстройств служит распад микротромбов в просвете периферических сосудов малого круга кровообращения. При разрушении полиморфно-ядерных лейкоцитов выделяются химические медиаторы воспаления (кинины, простагландины, комплементарные белки). По мере развития респираторного дистресс-синдрома снижается эластичность легочной ткани, уменьшается вентиляция легких и возрастает величина «шунтирования» крови. 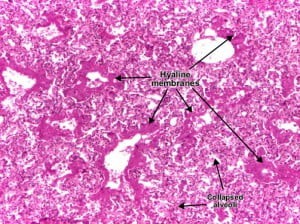 При морфологических исследованиях обнаруживают интерстициальный отек легкого, внутрисосудистые скопления тромбоцитов, инфильтрацию стенок альвеол лейкоцитами, образование гиалиновых мембран.
При морфологических исследованиях обнаруживают интерстициальный отек легкого, внутрисосудистые скопления тромбоцитов, инфильтрацию стенок альвеол лейкоцитами, образование гиалиновых мембран.
При сильном увеличении (электронная микроскопия) видны расширенные межклеточные промежутки в эндотелии сосудов, обнаженные базальные мембраны на границе альвеоло-капиллярных пространств.
Морфологические изменения при РДС различной этиологии идентичны (шок, интоксикации, сепсис и др.), что подтверждает общность легочного ответа на экстремальные воздействия.
Картина РДС проявляется не ранее 1 — 2 суток после травмы. Возникает одышка, появляется цианоз, нарушается ритм дыхания, которое приобретает стридорозный, клокочущий характер. Рентгенологически регистрируют признаки интерстициального и альвеолярного отека легких; контуры сердца нормальные.
Поздние случаи РДС сигнализируют о развитии гнойно-септического процесса. В таких наблюдениях РДС протекает с острой почечной недостаточностью (ОПН) и острой печеночной недостаточностью (ОПечН). Ранние формы РДС протекают изолированно.
К клинико-физиологическим признакам, подтверждающим РДС, относятся: гипоксемия (РаО² 60 мм рт. ст. и менее), снижение эластичности легких (комплайнс-тест менее 50), возрастание величины «мертвого» пространства и «шунтирования» крови в легких. Обогащение вдыхаемой смеси кислородом свыше 40% уже не может поддержать адекватной оксигенации крови. Для этого требуется ИВЛ в режиме положительного давления в конце выдоха (ПДКВ). Клинико-физиологическое разделение РДС на тяжелые и очень тяжелые формы основывается на частоте дыхания (больше или меньше 36 в 1 мин) и соотношении PaО²/FiО² (больше или меньше 300 мм рт. ст.).
Лечение респираторного дистресс-синдрома (РДС) бывает эффективным тогда, когда его проводят по нескольким линиям. Определенную роль играют общие поддерживающие меры: возвышенное положение груди и головного конца, систематическое изменение положения тела больного, физиотерапевтические процедуры на область груди, вибрационный массаж, максимальная активизация больного, постоянная стимуляция кашля, по возможности дыхательная гимнастика. При поздних формах РДС важны своевременная диагностика и хирургическое лечение очагов гнойно-септической инфекции, рациональный подбор антибиотиков. Инфузионно-трансфузионную терапию проводят с осторожностью, ограниченными объемами, желательно под контролем за давлением в легочной артерии. В предупреждении РДС наиболее эффективным методом признается ИВЛ в режиме ПДКВ (постоянная либо перемежающаяся принудительная вентиляция). При этом раскрывается максимальное количество альвеол, заметно улучшаются вентиляционно-перфузионные отношения. Чтобы избежать разрыва перерастянутых альвеол (баротравмы легких), избирают минимальную величину положительного давления на выдохе (от + 3 до +5 см вод. ст.) при величине жизненной емкости легких (ЖЕЛ) до 10 мл/кг.
Кортикостероиды при лечении РДС эффективны, когда их применяют в больших дозах (метилпреднизолон по 30 мг/кг не менее 2 раз в сутки внутривенно). Очень важна систематическая санация трахеобронхиального дерева.
Развитию РДС нередко предшествует ранняя посттравматическая пневмония. По-видимому, патогенетически эти два осложнения связаны друг с другом. Особенно часто к РДС приводит пневмония, развивающаяся на фоне грамотрицательной или стафилококковой бактериемии. Посттравматические пневмонии развиваются у 1/3 всех пострадавших от тяжелых и сочетанных травм. Они протекают с участием стафилококков, протея, псевдомонад, клебсиелл. С особым постоянством пневмония развивается через 3—5 дней после перевода на ИВЛ. Рентгенологическая диагностика РДС на фоне контузии легких, отека, ателектазов затруднительна. Нередкие ложноположительные ответы (20%) обусловлены накоплением секрета в трахеобронхиальном дереве. Еще чаще (35%) не распознаются имеющиеся воспалительные очаги в легких. К симптомам, подтверждающим развитие пневмонии, относятся повышение температуры тела, боли в груди (вовлечение в воспалительный процесс плевры), наличие в просвете трехеи гнойного экссудата, снижение эластичности легких, гипоксемия.